Hoe werkt CO in op het lichaam?
Fixatie op hemoglobine in het bloed
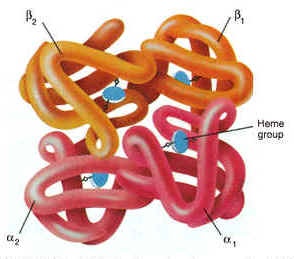
Hemoglobine
Bij de mens verzorgt hemoglobine, de kleurstof in de rode bloedcellen, het vervoer van zuurstof vanaf de longen tot aan de cellen.
Een hemoglobine-molecule is opgebouwd uit 4 polypeptide-ketens (globines) en bevat 4 heemgroepen, die elk een ijzeratoom (blauw) bevatten. De zuurstofmolecules hechten zich aan het ijzer.
De affiniteit van CO voor hemoglobine is 210 tot 260 keer hoger dan die van zuurstof. Zelfs bij aanwezigheid van minieme hoeveelheden, zal CO zich in plaats van zuurstof hechten aan de hemoglobine.
- Normaal: O2+ Hb → O2Hb (oxyhemoglobine)
- CO binding: CO + Hb → COHb (carboxyhemoglobine)
Zo wordt het zuurstoftransport naar de cellen verstoord en ontstaat er zuurstofgebrek ter hoogte van de cellen (cellulaire hypoxie).
De hoeveelheid carboxyhemoglobine die gevormd wordt hangt af van:
- De CO-concentratie in de lucht.
- De blootstellingsduur.
- De activiteitsgraad van het slachtoffer (hoe meer fysieke inspanningen, hoe sneller men ademt en hoe meer CO-gas men inademt).
- De algemene conditie van de persoon (hartproblemen, ziekten van het ademhalingsstelsel).
De binding van CO aan hemoglobine geeft niet alleen een vermindering van de hoeveelheid zuurstof, die per hemoglobinemolecule kan getransporteerd worden, maar heeft ook een indirecte invloed via de dissociatiecurve van oxyhemoglobine.
In de aanwezigheid van CO verplaatst de scheidingskromme van O2Hb in functie van de zuurstofspanning (PO2) zich naar links: CO neemt niet alleen de plaats in van de zuurstof op de hemoglobine, het verhoogt eveneens de affiniteit van hemoglobine voor zuurstof en verhindert de afgifte van zuurstof aan de periferie. De zuurstofspanning (PO2) in de perifere weefsels moet dus dieper dalen vooraleer de hemoglobine zuurstof zal afgeven. Dit vermindert nogmaals de hoeveelheid beschikbare zuurstof op celniveau.

Het dubbel mechanisme van verminderd transport naar en afgifte van zuurstof aan de cellen wordt geïllustreerd in bovenstaande figuur. In normale omstandigheden heeft het bloed de capaciteit om 5 ml zuurstof per 100 ml bloed aan de weefsels af te leveren bij een daling van de partiële zuurstofdruk van 60 mm Hg (van a naar V op de normale dissociatiecurve). In het geval van een bloedarmoede met een halvering van het aantal rode bloedcellen (halvering van de transportcapaciteit) vraagt de afgifte van 2,5ml zuurstof per 100ml bloed eenzelfde daling van de partiële zuurstofdruk van 60 mm Hg. In het geval van een CO intoxicatie met 50 % carboxyhemoglobine vraagt de afgifte van 2,5 ml zuurstof per 100 ml bloed een daling van de partiële zuurstofdruk van 75 mm Hg (van a’ naar V’).
Diffusie naar de weefsels
CO-gas wordt ook rechtstreeks in het bloedplasma opgenomen en penetreert op die manier in de weefsels. Dit in tegenstelling tot het CO dat op hemoglobine gebonden is, dat hier zodanig vast op gefixeerd is dat het bijna niet in de weefsels doordringt.
In de weefsels bindt CO zich aan de spiereiwitten (myoglobine). Myoglobine zorgt voor het zuurtoftransport in de spieren en het hart. Myoglobine heeft ook een grotere affiniteit (40 keer) voor CO dan voor zuurstof. Zoals voor hemoglobine, wordt de scheidingskromme, in aanwezigheid van CO, verplaatst naar links.
In de cellen bindt CO zich verder ook aan het cytochroom-c-oxidase dat verantwoordelijk is voor de oxidatie van cytochroom C in de ademhalingsketen van de mitochondriën. Als dit enzyme geblokkeerd is, ontstaat een anaëroob (zonder zuurstof) metabolisme (een echte “verstikking” van de cel) met de productie van melkzuur.
Door het onderbreken van de mitochondriale ademhalingsketen is er productie van vrije zuurstofradicalen. Gedurende de reoxygenatiefase kunnen vrije zuurstofradicalen hersenletsels veroorzaken door de peroxidatie van membraamlipiden. Men vermoedt dat de laattijdige hersenbeschadiging die men soms bij ernstige CO-intoxicatie aantreft, hierdoor veroorzaakt wordt.
CO fixeert zich ook op het cytochroom P450, een oxidatief enzym dat zich in bijna alle cellen bevindt, maar het exacte pathologische belang hiervan is nog niet gekend.